Fenómenos biofísicos-moleculares
Los fenómenos biofísicos moleculares son procesos que se realizan en los seres vivos, los cuales se basan en leyes físicas y físico-químicas dando lugar a la formación de dichos fenómenos. Los fundamentos moleculares de la Biofísica se rigen en las biomoléculas, o macromoléculas, y su funcionamiento en todo aspecto

- Fenómenos Químicos.
- Fenómenos Físicos.
- Fenómenos biofísicos-moleculares.
Fenómenos biofísicos-moleculares TENSIÓN SUPERFICIAL

Causa
A nivel microscópico, la tensión superficial se debe a que las fuerzas que afectan a cada molécula son diferentes en el interior del líquido y en la superficie. Así, en el seno de un líquido cada molécula está sometida a fuerzas de atracción que en promedio se anulan.
Esto permite que la molécula tenga una energía bastante baja. Sin embargo, en la superficie hay una fuerza neta hacia el interior del líquido. Rigurosamente, si en el exterior del líquido se tiene un gas, existirá una mínima fuerza atractiva hacia el exterior, aunque en la realidad esta fuerza es despreciable debido a la gran diferencia de densidades entre el líquido y gas.
Otra manera de verlo es que una molécula en contacto con su vecina está en un estado menor de energía que si no estuviera en contacto con dicha vecina. Las moléculas interiores tienen todas las moléculas vecinas que podrían tener, pero las partículas del contorno tienen menos partículas vecinas que las interiores y por eso tienen un estado más alto de energía. Para el líquido, el disminuir su estado energético es minimizar el número de partículas en su superficie.
Energéticamente, las moléculas situadas en la superficie tiene una mayor energía promedio que las situadas en el interior, por lo tanto la tendencia del sistema será disminuir la energía total, y ello se logra disminuyendo el número de moléculas situadas en la superficie, de ahí la reducción de área hasta el mínimo posible.
Como resultado de minimizar la superficie, esta asumirá la forma más suave que pueda ya que está probado matemáticamente que las superficies minimizan el área por la ecuación de Euler-Lagrange. De esta forma el líquido intentará reducir cualquier curvatura en su superficie para disminuir su estado de energía de la misma forma que una pelota cae al suelo para disminuir su potencial gravitacional.
Fenómenos biofísicos-moleculares Propiedades
La tensión superficial suele representarse mediante la letra griega (gamma), o mediante (sigma). Sus unidades son de N·m-1=J·m-2=Kg/s2=Dyn/
Algunas propiedades de:
- > 0, ya que para aumentar el estado del líquido en contacto hace falta llevar más moléculas a la superficie, con lo cual disminuye la energía del sistema y eso la cantidad de trabajo necesario para llevar una molécula a la superficie.
- depende de la naturaleza de las dos fases puestas en contacto que, en general, será un líquido y un sólido. Así, la tensión superficial será igual por ejemplo para agua en contacto con su vapor, agua en contacto con un gas inerte o agua en contacto con un sólido, al cual podrá mojar o no (véase capilaridad) debido a las diferencias entre las fuerzas cohesivas (dentro del líquido) y las adhesivas (líquido-superficie).
- se puede interpretar como un fuerza por unidad de longitud (se mide en N·m-1). Esto puede ilustrarse considerando un sistema bifásico confinado por un pistón móvil, en particular dos líquidos con distinta tensión superficial, como podría ser el agua y el hexano. En este caso el líquido con mayor tensión superficial (agua) tenderá a disminuir su superficie a costa de aumentar la del hexano, de menor tensión superficial, lo cual se traduce en una fuerza neta que mueve el pistón desde el hexano hacia el agua.
- El valor de depende de la magnitud de las fuerzas intermoleculares en el seno del líquido. De esta forma, cuanto mayor sean las fuerzas de cohesión del líquido, mayor será su tensión superficial. Podemos ilustrar este ejemplo considerando tres líquidos: hexano, agua y mercurio. En el caso del hexano, las fuerzas intermoleculares son de tipo fuerzas de Van der Waals. El agua, aparte de la de Van der Waals tiene interacciones de puente de hidrógeno, de mayor intensidad, y el mercurio está sometido al enlace metálico, la más intensa de las tres. Así, la de cada líquido crece del hexano al mercurio.
- Para un líquido dado, el valor de disminuye con la temperatura, debido al aumento de la agitación térmica, lo que redunda en una menor intensidad efectiva de las fuerzas intermoleculares. El valor de tiende a cero conforme la temperatura se aproxima a la temperatura crítica Tc del compuesto. En este punto, el líquido es indistinguible del vapor, formándose una fase continua donde no existe una superficie definida entre ambos, desapareciendo las dos fases. Al haber solamente una fase, la tensión superficial vale 0.
Fenómenos biofísicos-moleculares PRESIÓN HIDROSTÁTICA
La presión hidrostática es la fuerza por unidad de área que ejerce un líquido en reposo sobre las paredes del recipiente que lo contiene y sobre cualquier cuerpo que se encuentre sumergido, como esta presión se debe al peso del líquido, esta presión depende de la densidad (p), la gravedad (g) y la profundidad (h) del el lugar donde medimos la presión (P).
Un fluido pesa y ejerce presión sobre las paredes del fondo del recipiente que lo contiene y sobre la superficie de cualquier objeto sumergido en él. Esta presión, llamada presión hidrostática, provoca, en fluidos en reposo, una fuerza perpendicular a las paredes del recipiente o a la superficie del objeto sumergido sin importar la orientación que adopten las caras. Si el líquido fluyera, las fuerzas resultantes de las presiones ya no serían necesariamente perpendiculares a las superficies. Esta presión depende de la densidad del líquido en cuestión y de la altura del líquido con referencia del punto del que se mida.

Se calcula mediante la siguiente expresión:
- es la presión hidrostática (en pascales);
- es la densidad del líquido (en kilogramos partido metro cúbico);
- es la aceleración de la gravedad (en metros partido segundo al cuadrado);
- es la altura del fluido (en metros). Un líquido en equilibrio ejerce fuerzas perpendiculares sobre cualquier superficie sumergida en su interior
- es la Presión atmosférica (en pascales)
Fenómenos biofísicos-moleculares ADHESIÓN
La adhesión es la propiedad de la materia por la cual se unen y plasman dos superficies de sustancias iguales o diferentes cuando entran en contacto, y se mantienen juntas por fuerzas intermoleculares.
La adhesión ha jugado un papel muy importante en muchos aspectos de las técnicas de construcción tradicionales. La adhesión del ladrillo con el mortero (cemento) es un ejemplo claro.
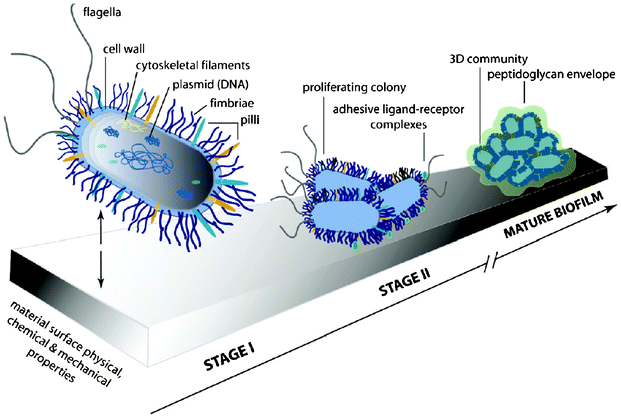
- Adhesión mecánica
Los materiales adhesivos rellenan los huecos o poros de las superficies manteniendo las superficies unidas por enclavamiento. Existen formas a gran escala de costura, otras veces a media escala como el velcro y algunos adhesivos textiles que funcionan a escalas pequeñas. Es un método similar a la tensión superficial
- Adhesión química
Dos materiales pueden formar un compuesto químico al unirse. Las uniones más fuertes se producen entre átomos donde hay permutación (enlace iónico) o se comparten electrones (enlace covalente). Un enlace más débil se produce cuando un átomo de hidrógeno que ya forma parte de una partícula se ve atraída por otra de nitrógeno, oxígeno o flúor, en ese caso hablamos de un puente.
- Adhesión dispersiva
En la adhesión dispersiva, dos materiales se mantienen unidos por las fuerzas de van der Waals: la atracción entre dos moléculas, cada una de las cuales tiene regiones de carga positiva y negativa. En este caso, cada molécula tiene una región de mayor carga positiva o negativa que se une a la siguiente de carga contraria. Este efecto puede ser una propiedad permanente o temporal debido al movimiento continuo de los electrones en una región.
En la ciencia de superficies el término «adhesión» siempre se refiere a una adhesión dispersiva. En un sistema sólido-líquido-gas normal (como una gota de un líquido sobre una superficie rodeada de aire) el ángulo de contacto es usado para cuantificar la adhesividad. En los casos donde el ángulo de contacto es bajo la adhesión está muy presente. Esto se debe a que una mayor superficie entre el líquido y el sólido conlleva una energía superficial mayor.
- Adhesión electrostática
Algunos materiales conductores dejan pasar electrones formando una diferencia de potencial al unirse. Esto da como resultado una estructura similar a un condensador y crea una fuerza electrostática atractiva entre materiales con diversos materiales les pueden ayudar.
Fenómenos biofísicos-moleculares COHESIÓN
Es la atracción entre moléculas que mantiene unidas las partículas de una sustancia. La cohesión es diferente de la adhesión; la cohesión es la fuerza de atracción entre partículas adyacentes dentro de un mismo cuerpo, mientras que la adhesión es la interacción entre las superficies de distintos cuerpos.

En el agua la fuerza de cohesión es elevada por causa de los puentes de hidrógeno que mantienen las moléculas de agua fuertemente unidas, formando una estructura compacta que la convierte en un líquido casi incompresible. Al no poder comprimirse puede funcionar en algunos animales como un esqueleto hidrostático, como ocurre en algunos gusanos perforadores capaces de agujerear la roca mediante la presión generada por sus líquidos internos.
La cohesión en los diferentes estados:
- Tanto los gases como los líquidos son fluidos, pero los líquidos tienen una propiedad de la que carecen los gases: tienen una superficie “libre”, o sea tienen una superficie cuya forma no está determinada por la forma del recipiente que lo contiene. Esta superficie se forma por una combinación de atracción gravitacional de la tierra (fuerza ocasionada por el peso) y de fuerzas entre moléculas del líquido. Una consecuencia de eso es que en la superficie de los líquidos actúa una fuerza que no está presente en el interior de los líquidos (salvo que haya burbujas en el interior), por eso llamada “tensión superficial”. Aunque relativamente pequeña, esta fuerza es determinante para muchos procesos biológicos, para la formación de burbujas, para la formación de olas pequeñas, etc.
- También en los gases, la fuerza de cohesión puede observarse en su licuefacción, que tiene lugar al comprimir una serie de moléculas y producirse fuerza de atracción suficientemente altas para proporcionar una estructura líquida.
- En los líquidos, la cohesión se refleja en la tensión superficial, causada por una fuerza no equilibrada hacia el interior del líquido que actúa sobre las moléculas superficiales, y también en la transformación de un líquido en sólido cuando se comprimen las moléculas lo suficiente. En los sólidos, la cohesión depende de cómo estén distribuidos los átomos, las moléculas y los iones, lo que a su vez depende del estado de equilibrio (o desequilibrio) de las partículas atómicas. Muchos compuestos orgánicos, por ejemplo, forman cristales moleculares, en los que los átomos están fuertemente unidos dentro de las moléculas, pero éstas se encuentran poco unidas entre sí.
En conclusión la cohesión se caracteriza así según el estado de las sustancias:
En los sólidos, las fuerzas de cohesión son elevadas y en las tres direcciones espaciales.
Cuando aplicamos una fuerza solo permite pequeños desplazamientos de las moléculas entre sí, cuando cesa la fuerza exterior, las fuerzas de cohesión vuelven a colocar las moléculas en su posición inicial.
Fenómenos biofísicos-moleculares
En los líquidos, las fuerzas de cohesión son elevadas en dos direcciones espaciales, y entre planos o capas de fluidos son muy débiles. Por otra parte las fuerzas de adherencia con los sólidos son muy elevadas. Cuando aplicamos una fuerza tangencial al líquido, este rompe sus débiles enlaces entre capas, y las capas de líquido deslizan unas con otras. Cuando cesa la fuerza, las fuerzas de cohesión no son lo suficiente fuertes como para volver a colocar las moléculas en su posición inicial, queda deformado. La capa de fluido que se encuentra justo en contacto con el sólido, se queda pegada a éste, y las capas de fluido que se encuentran unas juntas a las otras deslizan entre sí.
En los gases, las fuerzas de cohesión son despreciables, las moléculas se encuentran en constante movimiento. Las fuerzas de adherencia con los sólidos y los líquidos son importantes. Al aplicarse una fuerza de corte, se aumenta la velocidad media de las moléculas. Como estas partículas con más velocidad media (más cantidad de movimiento) se mueven en el espacio, algunas pasan a las capas contiguas aumentando a su vez la velocidad media de esas capas adyacentes, estas a su vez con una cantidad de movimiento más pequeña, algunas de sus partículas pasan a la capa de mayor cantidad de movimiento (afectada por el esfuerzo de corte) frenándola
Fenómenos biofísicos-moleculares DIFUSIÓN
La difusión (también difusión molecular) es un proceso físico irreversible, en el que partículas materiales se introducen en un medio que inicialmente estaba ausente, aumentando la entropía (Desorden molecular) del sistema conjunto formado por las partículas difundidas o soluto y el medio donde se difunden o disuelven.
Normalmente los procesos de difusión están sujetos a la Ley de Rick. La membrana permeable puede permitir el paso de partículas y disolvente siempre a favor del gradiente de concentración. La difusión, proceso que no requiere aporte energético, es frecuente como forma de intercambio celular.

Fenómenos biofísicos-moleculares Difusión simple
Se denomina difusión simple al proceso por el cual se produce un flujo neto de moléculas a través de una membrana permeable sin que exista un aporte externo de energía. Este proceso, que en última instancia se encuentra determinado por una diferencia de concentración entre los dos medios separados por la membrana; no requiere de un aporte de energía debido a que su principal fuerza impulsora es el aumento de la entropía total del sistema.
En este proceso el desplazamiento de las moléculas se produce siguiendo el gradiente de concentración, las moléculas atraviesan la membrana desde el medio donde se encuentran en mayor concentración, hacia el medio donde se encuentran en menor concentración.
El proceso de difusión simple se encuentra descrito por las Leyes de Fick, las cuales relacionan la densidad del flujo de las moléculas con la diferencia de concentración entre los dos medios separados por la membrana, el coeficiente de difusión de las mismas y la permeabilidad de la membrana.
El proceso de difusión simple es de vital importancia para el transporte de moléculas pequeñas a través de las membranas celulares. Es el único mecanismo por el cual el oxígeno ingresa a las células que lo utilizan como aceptor final de electrones en la cadena respiratoria y uno de los principales mecanismos de regulación osmótica en las células.
Fenómenos biofísicos-moleculares Difusión facilitada
Algunas moléculas son demasiado grandes como para difundir a través de los canales de la membrana y demasiado hidrofílicos para poder difundir a través de la capa de fosfolípidos y hopanoides. Tal es el caso de la fructosa y algunos otros monosacáridos.
Estas sustancias, pueden cruzar la membrana plasmática mediante el proceso de difusión facilitada, con la ayuda de una proteína transportadora. En el primer paso, la glucosa se une a la proteína transportadora, y esta cambia de forma, permitiendo el paso del azúcar. Tan pronto como la glucosa llega al citoplasma, una quinasa (enzima que añade un grupo fosfato a un azúcar) transforma la glucosa en glucosa-6-fosfato. De esta forma, las concentraciones de glucosa en el interior de la célula son siempre muy bajas, y el gradiente de concentración exterior → interior favorece la difusión de la glucosa.
La difusión facilitada es mucho más rápida que la difusión simple y depende:
- Del gradiente de concentración de la sustancia a ambos lados de la membrana.
- Del número de proteínas transportadoras existentes en la membrana.
- De la rapidez con que estas proteínas hacen su trabajo.
Difusión facilitada: la fuerza impulsora es el aumento de entropía por el aumento de concentración a un lado de la membrana. Tanto la difusión facilitada como el transporte activo se producen a través de proteínas integrales de membrana.
Fenómenos biofísicos-moleculares OSMOSIS
La ósmosis es un fenómeno físico relacionado con el movimiento de un solvente a través de una membrana semipermeable. Tal comportamiento supone una difusión simple a través de la membrana, sin «gasto de energía». La ósmosis del agua es un fenómeno biológico importante para el metabolismo celular de losares.

Fenómenos biofísicos-moleculares Mecanismo
Se denomina membrana semipermeable a la que contiene poros o agujeros, al igual que cualquier filtro, de tamaño molecular. El tamaño de los poros es tan minúsculo que deja pasar las moléculas pequeñas pero no las grandes, normalmente del tamaño de micrómetros. Por ejemplo, deja pasar las moléculas de agua, que son pequeñas, pero no las de azúcar, que son más grandes.
Si una membrana como la descrita separa un líquido en dos particiones, una de agua pura y otra de agua con azúcar, suceden varias cosas, explicadas a fines del siglo XIX por Van’t Hoff y Gibbs empleando conceptos de potencial electroquímico y difusión simple, entendiendo que este último fenómeno implica no sólo el movimiento al azar de las partículas hasta lograr la homogénea distribución de las mismas y esto ocurre cuando las partículas que vienen se equiparan con las que aleatoriamente van, sino el equilibrio de los potenciales químicos de ambas particiones. Los potenciales químicos de los componentes de una solución son menores que la suma del potencial de dichos componentes cuando no están ligados en la solución. Este desequilibrio, que está en relación directa con la os molaridad de la solución, genera un flujo de partículas solventes hacia la zona de menor potencial que se expresa como presión osmótica mensurable en términos de presión atmosférica, por ejemplo: «existe una presiónosmóticade50atmósferas entre agua desalinizada y agua de mar». El solvente fluirá hacia el soluto hasta equilibrar dicho potencial o hasta que la presión hidrostática equilibre la presión osmótica.1 2
El resultado final es que, aunque el agua pasa de la zona de baja concentración a la de alta concentración y viceversa, hay un flujo neto mayor de moléculas de agua que pasan desde la zona de baja concentración a la de alta.
Dicho de otro modo: dado suficiente tiempo, parte del agua de la zona sin azúcar habrá pasado a la de agua con azúcar. El agua pasa de la zona de baja concentración a la de alta concentración.
Las moléculas de agua atraviesan la membrana semipermeable desde la disolución de menor concentración, disolución hipotónica, a la de mayor concentración, disolución hipertónica. Cuando el trasvase de agua iguala las dos concentraciones, las disoluciones reciben el nombre de isotónicas.
En los seres vivos, este movimiento del agua a través de la membrana celular puede producir que algunas células se arruguen por una pérdida excesiva de agua, o bien que se hinchen, posiblemente hasta reventar, por un aumento también excesivo en el contenido celular de agua. Para evitar estas dos situaciones, de consecuencias desastrosas para las células, estas poseen mecanismos para expulsar el agua o los iones mediante un transporte que requiere gasto de energía.
La ósmosis es un fenómeno físico relacionado con el movimiento de un solvente a través de una membrana semipermeable. Tal comportamiento supone una difusión simple a través de la membrana, sin «gasto de energía». La ósmosis del agua es un fenómeno biológico importante para el metabolismo celular de losares.
Fenómenos biofísicos-moleculares ABSORCIÓN
Absorción es la operación unitaria que consiste en la separación de uno o más componentes de una mezcla gaseosa con la ayuda de un solvente líquido con el cual forma solución (un soluto A, o varios solutos, se absorben de la fase gaseosa y pasan a la líquida).
Este proceso implica una difusión molecular turbulenta o una transferencia de masa del soluto A través del gas B, que no se difunde y está en reposo, hacia un líquido C, también en reposo. Un ejemplo es la absorción de amoníaco A del aire B por medio de agua líquida C.

Al proceso inverso de la absorción se le llama empobrecimiento o des absorción; cuando el gas es aire puro y el líquido es agua pura, el proceso se llama des humidificación, la des humidificación significa extracción de vapor de agua del aire.
Fenómenos biofísicos-moleculares Elección del disolvente para absorción
Si el propósito principal de la operación de absorción es producir una solución específica, el disolvente es especificado por la naturaleza del producto. Si el propósito principal es eliminar algún componente del gas, casi siempre existe la posibilidad de elección. Por supuesto, el agua es el disolvente más barato y más completo, pero debe darse considerable importancia a las siguientes propiedades:
- Solubilidad del gas:
La solubilidad del gas debe ser elevada, a fin de aumentar la rapidez de la absorción y disminuir la cantidad requerida de disolvente.
En general, los disolventes de naturaleza química similar a la del soluto que se va a absorber proporcionan una buena solubilidad. Para los casos en que son ideales las soluciones formadas, la solubilidad del gas es la misma, en fracciones mol, para todos los disolventes.
Sin embargo, es mayor, en fracciones peso, para los disolventes de bajo peso molecular y deben utilizarse pesos menores de estos disolventes. Con frecuencia, la reacción química del disolvente con el soluto produce una solubilidad elevada del gas; empero, si se quiere recuperar el disolvente para volverlo a utilizar, la reacción debe ser reversible.
- Volatilidad:
El disolvente debe tener una presión baja de vapor, puesto que el gas saliente en una operación de absorción generalmente está saturado con el disolvente y en consecuencia, puede perderse una gran cantidad. Si es necesario, puede utilizarse un líquido menos volátil para recuperar la parte evaporada del primer disolvente.
- Corrosión:
Los materiales de construcción que se necesitan para el equipo no deben ser raros o costosos.
- Costo:
El disolvente debe ser barato, de forma que las pérdidas no sean costosas, y debe obtenerse fácilmente.
- Viscosidad:
Se prefiere la viscosidad baja debido a la rapidez en la absorción, mejores características en la inundación de las torres de absorción, bajas caídas de presión en el bombeo y buenas características de transferencia de calor.
- Otros:
Si es posible, el disolvente no debe ser tóxico, ni inflamable, debe ser estable químicamente y tener un punto bajo de congelamiento.
Absorción es la operación unitaria que consiste en la separación de uno o más componentes de una mezcla gaseosa con la ayuda de un solvente líquido con el cual forma solución (un soluto A, o varios solutos, se absorben de la fase gaseosa y pasan a la líquida).
Fenómenos biofísicos-moleculares ACCIÓN CAPILAR Y CAPILARIDAD
Atracción capilar, o capilaridad, es la capacidad de un líquido a fluir en espacios estrechos sin la ayuda de, y en oposición a fuerzas externas como la gravedad. El efecto puede ser visto en la elaboración de líquidos entre los pelos de un pincel, en un tubo delgado, en materiales porosos tales como papel, en algunos materiales no porosos tales como fibra de carbono licuado, o en una célula. Ocurre debido a fuerzas intermoleculares entre las superficies circundantes líquidas y sólidas. Si el diámetro del tubo es suficientemente pequeño, entonces la combinación de la tensión superficial y las fuerzas adhesivas entre el líquido y el acto de levantar el recipiente de líquido.
La capilaridad es un proceso de los fluidos que depende de su tensión superficial la cual, a su vez, depende de la cohesión del líquido y que le confiere la capacidad de subir o bajar por un tubo capilar.

Cuando un líquido sube por un tubo capilar, es debido a que la fuerza intermolecular o cohesión intermolecular entre sus moléculas es menor que la adhesión del líquido con el material del tubo; es decir, es un líquido que moja. El líquido sigue subiendo hasta que la tensión superficial es equilibrada por el peso del líquido que llena el tubo. Éste es el caso del agua, y esta propiedad es la que regula parcialmente su ascenso dentro de las plantas, sin gastar energía para vencer la gravedad
Sin embargo, cuando la cohesión entre las moléculas de un líquido es más potente que la adhesión al capilar, como el caso del mercurio, la tensión superficial hace que el líquido descienda a un nivel inferior y su superficie esconvexa.





